8 de Septiembre: Día Mundial de la Fibrosis Quística
La Federación Española de Fibrosis Quística, junto con el resto de países miembros de Asociación Internacional de FQ (Cystic Fibrosis Worldwide, CFW), celebran el Día Mundial desde 2013.
La fibrosis quística es una enfermedad hereditaria que provoca daños graves en los pulmones, el aparato digestivo y otros órganos del cuerpo. La fibrosis quística afecta las células que producen mucosidad, sudor y jugos digestivos. Estos líquidos secretados normalmente son ligeros y resbalosos. Sin embargo, en las personas que tienen fibrosis quística, es un gen defectuoso el responsable de que las secreciones sean más pegajosas y espesas. En lugar de actuar como lubricantes, las secreciones se acumulan en los tubos, conductos y pasajes, en particular en los pulmones y el páncreas.
¿Cuál es la causa?
En la fibrosis quística, un defecto (mutación) en un gen cambia una proteína que regula el movimiento de la sal al ingresar en las células y salir. El resultado es una mucosidad espesa y pegajosa en los aparatos respiratorio, digestivo y reproductivo, además de una mayor cantidad de sal en el sudor.
El tipo de mutación genética se asocia a la gravedad de la afección.
Los hijos deben heredar una copia del gen de cada padre para tener la enfermedad. Si solo heredan una copia, no tendrán fibrosis quística. Sin embargo, serán portadores y posiblemente les transmitan el gen a sus propios hijos.
Factores de riesgo
Antecedentes familiares. Dado que la fibrosis quística es un trastorno hereditario, se transmite de generación en generación.
Raza. Si bien la fibrosis quística se manifiesta en todas las razas, es más frecuente en personas blancas de origen noreuropeo.
¿Cómo se diagnostica?
Prueba del sudor
El diagnóstico de FQ se realiza mediante la cuantificación del contenido de sal en el sudor.
La prueba de sudor es confiable y no dolorosa, y su análisis requiere profesionales entrenados y experimentados, que realicen un número elevado de pruebas al año con la técnica de Gibson y Cooke.
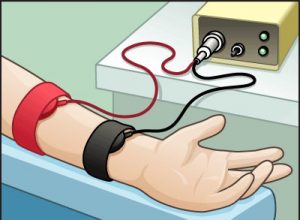
Generalmente se estimulan las glándulas sudoríparas de una zona del antebrazo con una sustancia (pilocarpina) y el paso de una corriente eléctrica débil (iontoforesis)
Se recoge el sudor y se determina el contenido de cloro y sodio. El procedimiento se completa en aproximadamente una hora
Debido a que la proteína CFTR está alterada o ausente y el transporte de cloruro se ve limitado, el sudor en una persona con FQ puede ser hasta cinco veces más salado que el de una persona sin la enfermedad.
Un resultado positivo de la prueba del sudor debe confirmarse y seguidamente se debe hacer un análisis de las mutaciones del gen de la FQ.
Mutación del gen de la fibrosis quística
El gen específico responsable de la FQ fue identificado en 1989 y hasta la fecha se han descubierto más de 1.000 mutaciones diferentes.
El descubrimiento del gen de la FQ ha posibilitado la identificación de individuos afectados y portadores, y ha contribuido a la comprensión de cómo y por qué se produce la enfermedad.
El American College of Medical Genetics (ACMG) y el American College of Obstetricians and Gynecologists (ACOG) recomiendan un panel que detecta 23 de las mutaciones más comunes del gen CFTR tanto en la población general como en poblaciones seleccionadas, para detectar así enfermos o portadores de la enfermedad.
La ACOG recomienda ofrecer el cribado de la FQ a todas las mujeres en edad fértil o embarazadas; en caso de que la madre sea portadora, debe realizarse el estudio en el padre biológico. La ACMG recomienda además realizar el análisis en otros familiares de riesgo. Si se identifican dos mutaciones causantes de FQ, una en cada uno de los progenitores, conviene que un consultor genético explique el riesgo relativo que la pareja tiene de concebir un hijo con FQ. Por otra parte, es muy importante recomendar también el consejo genético a todos los portadores y a personas con antecedentes familiares de FQ.
Pesquisa neonatal: Tripsina inmunoreactiva (IRT)
La FQ es una enfermedad de evolución progresiva y su pronóstico depende fundamentalmente de la oportunidad del diagnóstico. Existen evidencias claras que los niños diagnosticados mediante pesquisa neonatal (al nacer) y tratados adecuadamente, tienen mejor nutrición y función pulmonar que los diagnosticados por la presencia de síntomas.
La prueba de tripsina inmunorreactiva se basa en la observación que los recién nacidos afectados tienen concentraciones elevadas de esta enzima en sangre. La muestra debe obtenerse durante las primeras cuatro semanas de vida.
Se trata de un procedimiento de cribado para tripsinógeno en recién nacidos. El tripsinógeno se produce en el páncreas y se transporta al intestino donde se activa para formar la enzima tripsina. En la FQ, los tapones de moco espeso pueden obstruir los conductos pancreáticos e impedir el acceso del tripsinógeno al intestino. La concentración sanguínea de IRT puede estar elevada en recién nacidos con FQ, pero los resultados positivos deben confirmarse con otra prueba.
Tripsina y quimotripsina
Se trata de una prueba que se realiza en heces para detectar enzimas proteolíticas, que se producen de forma inactiva en el páncreas y se activan posteriormente en el intestino delgado para así digerir las proteínas de la dieta. Un resultado positivo indica normalidad. Es una prueba para el cribado de la suficiencia pancreática.
Detección de la Mutación DF508 para Fibrosis Quística
Suele haber importantes diferencias en el grado de afectación según las mutaciones que posee cada paciente.
La mutación más frecuente es la DF508; la frecuencia del resto es baja y muchas de ellas han sido halladas en grupos familiares únicos, por lo que es imposible el estudio de todas las mutaciones conocidas. Los pacientes portadores de DF508 presentan insuficiencia pancreática y altos niveles de cloruros en el sudor, y la mayoría tiene compromiso pulmonar que es variable en cuanto a severidad. En cambio, aquellos afectados con otras mutaciones pueden conservar cierta actividad del canal del cloro y las manifestaciones ser menos severas. No obstante, como ha sido mencionado, la evolución clínica es variable aún entre hermanos.
En nuestro país se observa que DF508 está presente en el 57% de los cromosomas Fq.
Fuente: Lab Tests Online – Mayo Clinic

Noticias más leídas